Navegación
Navegación Beatriz Suárez Álvarez1, Antonio López Vázquez1, Beatriz Díaz Molina2 y Carlos López-Larrea1.
1Unidad de Histocompatibilidad y Trasplantes. HUCA, Oviedo.
2Servicio de Cardiología, HUCA, Oviedo. inmuno@hca.es
Como consecuencia del trasplante de órganos sólidos se originan anticuerpos dirigidos principalmente frente a las moléculas de HLA de clase I y II. Estos anticuerpos juegan un papel fundamental en el rechazo del injerto.
Las moléculas MHC no clásicas MICA y MICB, muestran homología con HLA de clase I, pero no juegan un papel en la presentación antigénica. El hecho de que MICA (y MICB) se expresen en al superficie de las células endoteliales, sugiere que esta molécula pueda jugar un papel como posible diana humoral y celular en relación con la respuesta inmune generada durante el rechazo. La expresión de MICA es inducida en situaciones de estrés, en procesos infecciosos y durante transformación tumoral. Esta molécula es un ligando de las células NK y T CD8+, las cuales expresan el receptor NKG2D que ejercen su función a través de la molécula adaptadora DAP10. El receptor NKG2D actúa como un receptor de activación en NKs y como una señal coestimuladora del receptor TCR en linfocitos T CD8+.
Estudios preliminares han valorado la existencia de anticuerpos anti-MICA en relación con el rechazo. Se ha demostrado mediante test de ELISA y de citotoxicidad dependiente de complemento que durante el curso del trasplante renal se producen anticuerpos anti-MICA, aunque se desconoce el significado clínico de los mismos. Pacientes que habían recibido un trasplante renal/pancreático y habían desarrollado rechazo agudo o crónico, presentaban un incremento de la expresión de MICA en el órgano trasplantado y anticuerpos anti-MICA en el suero. Sin embargo, no es fácil establecer si MICA juega un papel en el rechazo de órganos debido a la presencia de anticuerpos anti HLA durante el periodo postransplante. Uno de los objetivos del nuestro trabajo consistió en evaluar si la presencia de aloanticuerpos anti-MIC puede ser la causa de rechazo agudo de ausencia de anticuerpos anti-HLA.
Con estos antecedentes, nos propusimos estudiar en pacientes trasplantados de corazón, el posible papel de MICA en los mecanismos de regulación de la respuesta inmune que ocurren tras el trasplante y su posible contribución a una mejor tolerancia del injerto.
Para la realización de este estudio de selecciono un grupo de 43 pacientes con trasplante cardíaco procedentes del Hospital Universitario Central de Asturias de Oviedo y del Hospital "Virgen de la Arrixaca" de Murcia.
La presencia de MICA soluble puede condicionar la aparición de rechazo agudo en trasplante cardíaco
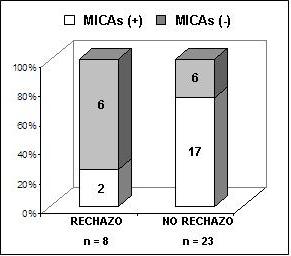
La presencia de MICA soluble (MICAs) se detectó usando técnicas de ELISA en el suero de pacientes trasplantados, obtenidos a diferentes tiempos, durante el primer año post-trasplante. MICAs se detectó en el suero del 61% de los pacientes analizados a los 15-20 días post-trasplante. El análisis de los datos clínicos reveló que el 74% de los pacientes que no desarrollaron episodios de rechazo agudo severo durante el primer año tienen MICAs (p<0.03), mientras que sólo 2 de los pacientes con rechazo presentaban la proteína en suero. La correlación entre la presencia de MICAs en el suero de pacientes trasplantados y la ausencia de rechazo se mantuvo durante el primer año post-trasplante en el 80% de los pacientes.
Se puede concluir que la presencia de MICAs se correlaciona directamente con la ausencia de episodios de rechazo agudo durante el primer año postrasplante.
La proteína MICA se comporta como un aloantígeno de trasplante
El siguiente paso en el desarrollo de este proyecto fue detectar la presencia de anticuerpos específicos frente a MICA en el suero de los pacientes con trasplante cardíaco. Para ello se desarrolló una técnica de citotoxicidad dependiente de complemento utilizando líneas celulares recombinantes humanas, transfectadas con los 7 alelos de MICA más comunes en la población caucasoide.
El 29% de los pacientes trasplantados desarrollaron anticuerpos anti-MICA específicos de alelo mientras que sólo 2 individuos tenían anticuerpos anti-HLA clase I post-trasplante. Además, la presencia de anticuerpos anti-MICA fue significativamente más alta en pacientes con rechazo agudo severo durante el primer año (p<0.03).
Por tanto, la presencia de anticuerpos anti-MICA post-trasplante podría contribuir al desarrollo de rechazo agudo del injerto en pacientes con trasplante cardiaco. Además, el análisis combinado de la presencia de MICAs y de anticuerpos anti-MICA, indica que los pacientes con MICAs podrían tener una mejor aceptación del órgano en ausencia de anticuerpos anti-MICA
Aumento de la expresión de MICA en biopsias de pacientes con evidencia histológica de rechazo agudo
La fase final de nuestro estudio consistió en analizar la expresión de MICA, a nivel de proteína y de RNA mensajero (mRNA), en biopsias endomiocardicas de 10 pacientes, obtenidas a diferentes tiempos durante el primer año post-trasplante. Para ello se emplearon técnicas inmunohistoquímica y de RT-PCR "real-time".
Los niveles de mRNA fueron más altos en biopsias con rechazo agudo que en aquellas que no presentaban evidencia histológica de este. En la mayoría de los casos, la expresión de MICA estaba incrementada inmediatamente después del trasplante independientemente del rechazo, sugiriendo una sobre-expresión probablemente debida a estrés celular. El análisis inmunohistoquímico mostró la ausencia de tinción para MICA en los pacientes sin rechazo, observándose sin embargo una tinción intensa y difusa en el citoplasma de cardiomiocitos en pacientes con rechazo agudo.
En conclusión, nuestros resultados indican que la monitorización post-trasplante de MICA (soluble y en membrana) así como de anticuerpos anti-MICA pueden ser de gran ayuda en el diagnostico del rechazo agudo severo e incluso pueden permitir el desarrollo de nuevas terapias inmunomoduladoras que faciliten su control.
Bibliografía
Terasaki P. Humoral theory transplantation. Am. J. Transplantation 2003;3:665-673.
Bahram S, Bresnahan M, Geraghty DE, Spies T. A second lineage of mammalian major histocompatibility complex class I genes. Proc Natl Acad Sci USA. 1994;91:6259-6263.
Suárez-Alvarez B, Lopez-Vazquez A, Diaz-Molina B, Bernardo-Rodriguez MJ, Álvarez-López R, Pascual D, Astudillo A, Martínez-Borra J, Lambert JL, González S, López-Larrea C. The predictive value of soluble major histocompatibility complex class I chain-related molecule A (MICA) levels on heart allograft rejection. Transplantation. 2006 ;82(3):354-61.
Suárez-Álvarez B, López-Vazquez A, Díaz-Pena R, Díaz-Molina B, Blanco-García RM, Álvarez-López MR, López-Larrea C. Post-transplant soluble MICA and MICA antibodies predict subsequent heart grafo outcome. Transpl Immunol. 2006 ;17(1):43-6.
Suárez-Álvarez B, López-Vázquez A, Zapico González M, Fdez-Morera JL, Díaz-Molina B,. Blanco-Gelaz MA, Pascual D, Martínez-Borra J, Muro M, Álvarez-López MR, López-Larrea C. The relationship of anti-MICA antibodies and MICA expression with heart allograft rejection. American Journal of Transplantation 2007 (en prensa).
Beatriz Suárez Álvarez1, Antonio López Vázquez1, Beatriz Díaz Molina2 y Carlos López-Larrea1.
Destacados
- Volumen y resultados: ¿es hora de un paso adelante en la regionalización de la cirugía?
- Prescripción potencialmente inadecuada en dos centros socio-sanitarios según los criterios START-STOPP
- Guía Farmacoterapéutica (GFT) unificada para hospitales del Servicio de Salud del Principado de Asturias
- Sistema de vigilancia del cáncer laboral en el Principado de Asturias Nota 1: Programa de detección y comunicación de cáncer profesional
- Biblioteca del Hospital Universitario Central de Asturias
Sugeridos desde E-Notas
- Radiocirugía estereotáctica para el tratamiento de la epilepsia, el temblor esencial, la enfermedad de Parkinson, la neuralgia del glosofaríngeo y del trigémino. Síntesis de su eficacia, efectividad, seguridad y eficiencia
- Evaluación de la seguridad, eficacia, efectividad y eficiencia de la teleconsulta en Atención Primaria, y de los aspectos organizativos, éticos, sociales y legales ligados a su uso
- Fármacos sedantes-hipnóticos para el tratamiento del trastorno de insomnio crónico primario
- DYNAMIC HEALTH: recurso de síntesis de evidencia para enfermería
- Evaluación de Tecnologías Sanitarias de Cirugía Metabólica para el Tratamiento de diabetes tipo 2 comórbida y Obesidad